প্রতীকের পাশে উল্লেখিত ভরসংখ্যাবিশিষ্ট মৌলের নিউট্রন সংখ্যা, বাের মডেল অনুসারে পরমাণুর গঠনের চিত্র, শক্তিস্তরে ইলেকট্রন বিন্যাস এবং উপশক্তিস্তরে (অরবিটালসমূহে) ইলেকট্রন বিন্যাস সংশ্লিষ্ট একটি প্রতিবেদন প্রণয়ন
স্তরঃ এস.এস.সি পরীক্ষা ২০২১
বিভাগঃ বিজ্ঞান
বিষয়ঃ রসায়ন
বিষয় কোডঃ ১৩৭
মোট নম্বরঃ ১০
অ্যাসাইনমেন্ট নম্বর-০১
অধ্যায় ও অধ্যায়ের শিরােনামঃ তৃতীয়, পদার্থের গঠন।
অ্যাসাইনমেন্টঃ প্রতীকের পাশে উল্লেখিত ভরসংখ্যাবিশিষ্ট মৌলের নিউট্রন সংখ্যা, বাের মডেল অনুসারে পরমাণুর গঠনের চিত্র, শক্তিস্তরে ইলেকট্রন বিন্যাস এবং উপশক্তিস্তরে (অরবিটালসমূহে) ইলেকট্রন বিন্যাস সংশ্লিষ্ট একটি প্রতিবেদন প্রণয়ন।
Na(11), ভরসংখ্যা -23 P(15), ভরসংখ্যা -31 K(19), ভরসংখ্যা -40 Cu(29), ভরসংখ্যা -63
শিখনফল/বিষয়বস্তুঃ
১. পরমাণু ইলেকট্রন, প্রােটন ও নিউট্রন সংখ্যা হিসাব করতে পারব। ২. পরমাণুর গঠন সম্পর্কে রাদারফোর্ড ও বাের পরমাণু মডেলের বর্ণনা করতে পারব। ৩. পরমাণুর বিভিন্ন কক্ষপথ এবং কক্ষপথের বিভিন্ন উপস্তরে পরমাণুর ইলেকট্রনসমূহকে বিন্যাস করতে পারব।
নির্দেশনা (সংকেত/ধাপ/পরিধি):
৪টি মৌলের নিউট্রন সংখ্যার হিসাব বের করতে হবে। ৪টি মৌলের বাের মডেল অনুসারে পরমাণুর গঠনের চিত্র অংকন করতে হবে ৪টি মৌলের শক্তিস্তরে ইলেকট্রন বিন্যাস করতে হবে ৪টি মৌলের উপশক্তিস্তরে (অরবিটালসমূহে) ইলেকট্রন বিন্যাস করতে হবে।
অধ্যায় ৩
পদার্থের গঠন
অ্যাসাইনমেন্ট : প্রতীকের পাশে উল্লেখিত ভরসংখ্যাবিশিষ্ট মৌলের নিউট্রন সংখ্যা, বোর মডেল অনুসারে পরমাণুর গঠনের চিত্র, শক্তস্তরে ইলেকট্রন বিন্যাস এবং উপশক্তিস্তরে (অরবিটালসমূহে) ইলেকট্রন বিন্যাস সংশ্লিষ্ট একটি প্রতিবেদন প্রণয়ন।
Na(11), ভরসংখ্যা -23
P(15), ভরসংখ্যা -31
K(19), ভরসংখ্যা -40
Cu(29), ভরসংখ্যা -63
নমুনা সমাধান
(ক)
নিউট্রন সংখ্যা হিসাব :
Na মৌলের নিউট্রন সংখ্যা =23−11=12
P মৌলের নিউট্রন সংখ্যা =31−15=16
K মৌলের নিউট্রন সংখ্যা =40−19=21
Cu মৌলের নিউট্রন সংখ্যা =63−29=34
(খ)
বোর মডেল অনুসারে পরমানুর গঠনের চিত্র অঙ্কন :
𝑁𝑎Na এর ইলেকট্রন বিন্যাস-


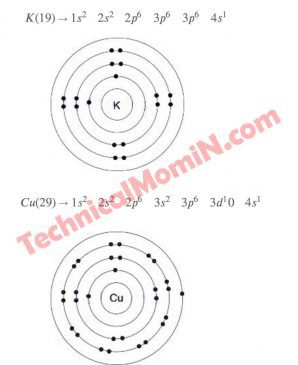

(গ)
শক্তিস্তরে ইলেকট্রন বিন্যাস


উপশক্তিস্তরে (অরবিটাল সমূহে) ইলেকট্রন বিন্যাস –
আমরা জানি,
n=1 এর জন্য উপশক্তিস্তর ০ থেকে (n−1) পর্যন্ত।
তাই প্রথম শক্তিস্তরে একটি উপশক্তিস্তর বিদ্যমান =1𝑠
𝑛=2 হলে, উপশক্তিস্তর হল = 2𝑠, 2p
n=3 হলে, উপশক্তি স্তর হল = 3𝑠, 3p, 3d
n=4 হলে, উপশক্তি স্তর হল = 4s, 4p, 4d, 4f
s উপশক্তিস্তরে থাকে সর্বোচ্চ ২টি ইলেকট্রন।
𝑝 উপশক্তিস্তরে থাকে সর্বোচ্চ ৬টি ইলেকট্রন।
d উপশক্তিস্তরে থাকে সর্বোচ্চ ১০টি ইলেকট্রন।
f উপশক্তিস্তরে থাকে সর্বোচ্চ ১৪টি ইলেকট্রন।
পরমাণুর অরবিটালের ক্রমবর্ধমান শক্তিগুলো :
1𝑠 <2𝑠 <2𝑝 <3𝑠< 3𝑝 <4𝑠 <3𝑑


এসএসসি প্রথম সপ্তাহের এসাইনমেন্ট ২০২১
বাংলাদেশের ইতিহাস ও বিশ্বসভ্যতা
Finance and Banking 1st Week Assignment Answer
Biology 1st Week Assignment Answer
Business Entrepreneurship 1st Week Assignment Answer
৯ম শ্রেণীর ৯ম সপ্তাহের সকল অ্যাসাইনমেন্ট উত্তর
এস এস সি ( SSC ) দ্বিতীয় সপ্তাহের সকল এসাইনমেন্ট উত্তর
বাংলাদেশ ও বিশ্বপরিচয় এসাইনমেন্ট উত্তর
ইংরেজি এসাইনমেন্ট উত্তর
পদার্থ বিজ্ঞান এসাইনমেন্ট উত্তর
হিসাব বিজ্ঞান এসাইনমেন্ট উত্তর
অর্থনীতি এসাইনমেন্ট উত্তর
পৌরনীতি ও সুশাসন এসাইনমেন্ট উত্তর
যুক্তিবিদ্যা এসাইনমেন্ট উত্তর
তাছাড়া আমাদের ওয়েবসাইটে ( Class 6 ) ষষ্ঠ শ্রেণীর অ্যাসাইনমেন্ট , ( Class 7 ) সপ্তম শ্রেণীর অ্যাসাইনমেন্ট ( Class 8 ) অষ্টম শ্রেণীর অ্যাসাইনমেন্ট , (Class 9) নবম শ্রেণীর অ্যাসাইনমেন্ট, (SSC ) দশম শ্রেণীর অ্যাসাইনমেন্ট ( HSC ) একাদশ শ্রেণীর অ্যাসাইনমেন্ট উত্তর দেওয়া হয়ে থাকে আপনারা চাইলে দেখতে পারেন ।
